张永明医生的科普号
- 医学科普 出现疑似新型冠状病毒症状,哪些情况必须就诊?
满足以下任意一点即为存在重症风险,甚至已经出现重症情况。建议医院发热门诊就诊,必要时联系120并描述呼吸及神志情况。 (1)65岁以上的老年人; (2)体温>38℃; (3)有慢性基础疾病:心脏病、哮
张永明 副主任医师 中日医院 呼吸与危重症医学科1.4万人已读 - 医学科普 出现哪些症状才要怀疑感染了新型冠状病毒?
近期到过武汉或者湖北其他疫区,或者近距离与疫区归来的人员或疑似患者有过近距离接触的,出现相关症状应该怀疑新型冠状病毒的感染。 ①发热:以高热症状为最典型。发热的同时常伴有肌肉酸痛和全身乏力,不典型病例
张永明 副主任医师 中日医院 呼吸与危重症医学科21.7万人已读 - 医学科普 如何正确区分是得了普通感冒还是新型冠状病毒
普通感冒早期可出现畏寒,咽部干痒或灼热感,伴随打喷嚏、鼻塞、流涕,开始为清水样鼻涕,2~3天后变稠,可伴有咽痛。一般没有发热及全身症状,或仅有低热、头痛。一般不会出现咳嗽和气短。服用复方感冒药或者对症药物后一般三天内症状明显减轻,如无并发细菌感染,一般5~7天可痊愈。 新型冠状病毒患者绝大多数有发热,以高热症状为最典型。发热的同时常伴有肌肉酸痛和全身乏力。这种表现和流感相似。不典型病例为低热或者发热不明显。咳嗽、气短是较常见的症状,咳嗽一般以干咳为主,并伴有气短和逐渐加重的呼吸困难。其他少见症状还包括有咳痰、头痛、咯血和腹泻。多半患者出现血常规淋巴细胞减少。重症患者CT上均表现为肺炎,一般为双侧多发的肺炎。
张永明 副主任医师 中日医院 呼吸与危重症医学科18.1万人已读 - 引用 如何在家拍出清晰影像照片给我看
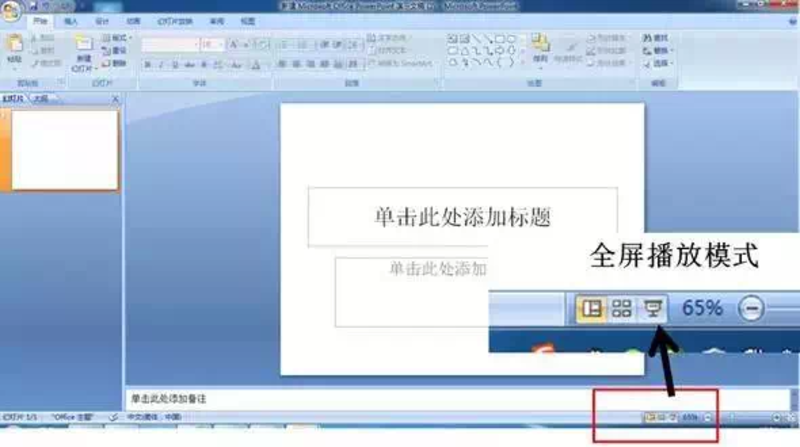
步骤一:电脑屏幕变“阅片灯” 打开电脑,新建一个PPT(幻灯片); 点击幻灯,在电脑右下角处点击全屏播放按钮,这时电脑屏幕摇身一变成为阅片灯。 步骤二:确定片子的正反顺序 把X光或CT片放在“电脑屏幕”上; 确保片子上的文字是顺的,就说明片子方向是正确的; 用胶布把片子固定在电脑屏幕上,片子可以清晰的显示! 步骤三:关闭手机闪光灯排版 用手机的相机拍照时要关闭“闪光灯”; 建议把一张片子分成几部分拍,最好“四格”一张,甚至可以一格一张,保证图像的清晰度,然后按顺序发送“原图”。
 于灏 副主任医师 中国医大一院 骨科3157人已读
于灏 副主任医师 中国医大一院 骨科3157人已读 - 医学科普 支气管哮喘 诊断评估和治疗GINA 指南解读张永明 副主任医师 中日医院 呼吸与危重症医学科2232人已读
- 医学科普 隐源性机化性肺炎(COP,BOOP)诊断治疗最新研究进展
隐源性机化性肺炎(闭塞性细支气管炎伴机化性肺炎,COP,BOOP)的诊断和治疗最新研究进展引言—隐源性机化性肺炎(cryptogenic organizing pneumonia, COP),属于特发性机化性肺炎[以往称为闭塞性细支气管炎伴机化性肺炎(bronchiolitis obliterans organizing pneumonia, BOOP)],是一种弥漫性间质性肺疾病,病变累及细支气管远端、呼吸性细支气管、肺泡管和肺泡壁。肺泡壁是损伤的主要区域。除了COP,还可见与结缔组织病、多种药物、恶性肿瘤及其他间质性肺炎有关的继发性机化性肺炎(organizing pneumonia, OP)。流行病学—COP确切的发病率和患病率尚未知。加拿大的一家大型教学医院发现,该病的累积发病率为6-7例/100,000次住院;而在冰岛,对20年国家统计资料进行回顾显示,年平均发病率为1.1/100,000。在其他报告中,56%-68%的OP病例被认为是隐源性而非继发性的。病理学—COP的特征性组织病理学表现包括肉芽组织过度增生,其中包括埋入疏松的胶原中的成纤维细胞和肌成纤维细胞,累及肺泡管和肺泡,伴或不伴细支气管腔内息肉。管腔内的肉芽组织栓可能通过肺泡间孔从一个肺泡延伸到相邻的肺泡,从而形成特征性的蝴蝶样结构。细支气管病变被认为是管腔内肉芽组织栓从肺泡囊和肺泡管扩展到细支气管的结果。其他病理特征包括受累区域内病变外观均匀,以及没有严重肺结构破坏的斑片状区域。病理性病变主要位于气腔内,肺泡壁存在轻度慢性炎症(例如,淋巴细胞和浆细胞浸润)。OP的组织学特征也可见于其他IIP。但相对于其他间质性肺炎的特征性改变,提示OP的改变占比较小(<10%)。发病机制—COP的确切发病机制尚不清楚。一般认为OP是肺泡上皮损伤的结果。初始损伤后,血浆蛋白渗出、成纤维细胞募集以及肺泡腔内纤维蛋白形成。有报道称COP与血管内皮生长因子和基质金属蛋白酶的异常调节有关。不过,在许多其他肺疾病中也可观察到这些蛋白质的失调,其在COP发病机制中的确切作用仍仅为推测性的。相比寻常型间质性肺炎中的不可逆性病变,COP中血管生成和细胞凋亡的调节可能影响纤维化病变的可逆性。学者已提出,胃食管反流病(gastroesophageal reflux disease, GERD)患者的胃分泌物微量误吸与OP之间可能存在关联。临床特征—COP起病通常是在40-49岁或50-59岁,男女患者数量相当。罕见儿童罹患COP。报道的当前吸烟或既往吸烟比例为25%-50%,因此吸烟不太可能是促发因素。病史—COP通常表现为咳嗽、呼吸困难、发热和不适,这些症状持续时间相对较短,例如几周到几个月。在几乎3/4的患者中,症状持续不到2个月。半数患者起病前会出现急性发作的流感样疾病,表现为发热、不适、乏力和咳嗽,而其他患者的症状发作稍缓。在部分患者中,经验性抗生素治疗社区获得性肺炎无效可能是提示存在非感染性、炎症性肺炎的最初线索。就诊时最常见的病史特征有:●持续性干咳(72%)●呼吸困难(66%)●发热(51%)●不适(48%)●体重减轻大于10磅(57%)很少有患者报告咯血为COP的主诉症状。正如对待所有间质性肺疾病患者一样,询问病史应包括任何提示结缔组织病的症状或病史(如,关节痛、眼干、口干、肌无力、麻木、麻刺感),当前和近期用药史,以及放疗、烟雾或粉尘的暴露史。表中列出了与继发性OP有关的疾病和药物。体格检查—对于COP患者,体格检查经常可闻及吸气相湿啰音(74%)。很少闻及哮鸣音,如果有,也常与湿啰音合并存在;在不到5%的病例中可见杵状指。1/4的患者肺部体格检查结果正常。鉴于OP与许多结缔组织病有关,应检查患者有无这些疾病的肺外表现,如脱发、Gottron征、向阳性皮疹、肌无力或压痛、肢端硬化以及甲襞毛细血管镜检查异常。这些特征的识别将单独介绍。评估—疑似COP患者的评估通常首先是针对呼吸困难和/或咳嗽症状进行胸片检查。胸片表现或抗生素治疗临床无效往往会提示进一步检查以排除非典型感染、恶性肿瘤以及可能与弥漫性肺实质疾病有关的全身疾病。这些检查通常包括实验室检查、高分辨率计算机断层扫描(high resolution computed tomography, HRCT)、肺功能检查、支气管肺泡灌洗(bronchoalveolar lavage, BAL)以及经支气管镜肺活检或外科肺活检。间质性肺疾病的评估将单独讨论。实验室检查—实验室检查对诊断COP没有特异性。然而,在评估存在呼吸困难、咳嗽、发热和影像学示肺部阴影的患者时,一般实验室检查包括全血细胞计数和分类计数、血尿素氮、肌酐、肝功能检查以及尿液分析。约50%的COP患者可见白细胞增多。初始ESR升高(经常达到或超过100mm)以及C反应蛋白阳性均见于70%-80%的患者,但我们不常规进行这些检查。对于临床表现提示社区获得性肺炎的住院患者,通常进行额外的检查,如血培养、痰革兰染色、痰酶免疫测定(enzyme immunoassay, EIA)、免疫荧光法,或PCR检测呼吸道病毒,尿液检查查找肺炎球菌和军团菌抗原,以及HIV检测。因为OP的发生也可能与多种结缔组织病有关,所以当根据症状或体征怀疑结缔组织病时,针对这些疾病开展检查是合理的,如抗核抗体、类风湿因子、肌酸激酶、抗拓扑异构酶抗体(抗-Scl70抗体)、抗着丝粒抗体、抗双链DNA抗体以及抗JO1抗体。COP患者(即不合并结缔组织病时)的自身抗体通常为阴性或滴度极低。在间质性肺疾病情况下识别潜在结缔组织病的实验室检查将单独讨论胸部影像学检查胸片—几乎所有持续存在呼吸困难和咳嗽的成人均应进行胸片检查,尤其是存在发热的个体。COP的胸片表现通常很有特征,表现为双侧斑片状或弥漫性实变影或磨玻璃影,并且肺容积正常。其他表现可能包括:●阴影分布于周边部位,类似于慢性嗜酸性粒细胞性肺炎(chronic eosinophilic pneumonia, CEP)。●常见复发性或游走性肺部阴影(在一些病例系列研究中,可见于多达50%的受试者)。●罕见情况下,单侧实变影和磨玻璃影。●罕见情况下,胸片发现仅为不规则线状或结节状阴影。●其他罕见的放射影像学异常包括胸腔积液、胸膜增厚、肺充气过度和肺空洞。CT扫描—通常行HRCT肺扫描进一步评估常规胸片上发现的异常。罕见情况下,患者可能存在呼吸困难和低氧血症或弥散量(DLCO)降低但胸片无明确异常,此时也可行HRCT评估气体交换异常。HRCT结果也用于指导选择行BAL或肺活检的部位。COP患者行HRCT显示的病变范围往往比根据阅读胸片所预期的范围更广。放射影像学改变包括斑片状气腔实变、磨玻璃影、小结节影,以及支气管壁增厚伴扩张。斑片状阴影更常见于肺的外周,常常位于下肺区。不太常见的放射影像学表现包括:可能内有空洞的多发结节或肿块、微小结节、胸膜下不规则网状阴影,以及新月形或环形阴影。罕见情况下,OP的唯一表现为单个结节,这种情况称为局灶性OP。据一项病例系列研究报道,在16例COP患者中,有6例出现纵隔淋巴结肿大(短轴直径≥10mm)。胸腔积液并不常见。因为COP与CEP都好发于外周肺野,因此要从影像学上明确区分两者往往不可能。肺功能测定—大多数表现出呼吸困难和咳嗽的门诊成人患者都进行肺功能测定,以确定症状是否与阻塞性或限制性通气障碍相关,以及是否存在气体交换障碍。肺功能受损的严重程度可作为是否需要进行侵袭性诊断性检查的决定因素之一。轻度至中度限制性通气障碍是COP最常见的表现。然而,一份报告显示20%的患者存在阻塞性通气障碍[第1秒用力呼气容积(forced expiratory volume in one second, FEV1)/用力肺活量(forced vital capacity, FVC)比值小于70%],这些患者都是目前或既往吸烟者。肺容积和肺流量的测量结果偶尔正常。气体交换异常极其常见。大多数患者的DLCO降低。超过80%的受试者存在静息和/或运动状态下动脉低氧血症(定义为肺泡-动脉氧分压差大于20mmHg)。静息状态时,脉搏血氧饱和度(SpO2)可能正常或降低,但劳力状态下通常降低。可屈性支气管镜—可屈性支气管镜常用于获取BAL标本以评估感染、出血和恶性肿瘤。有时在操作过程中取活检组织行组织病理学和微生物学检查,但标本量一般较小,不足以做出COP的明确诊断。或者,当感染的诊断不太可能或需要加快诊断过程时,可直接进行外科肺活检。支气管肺泡灌洗—COP患者的BAL检测结果并无特异性,所以BAL的主要作用在于识别亚急性起病的咳嗽、呼吸困难以及放射影像学上阴影这些表现的鉴别诊断范畴中的各种情况,如肺泡出血、恶性肿瘤或机会性感染。BAL技术和灌洗标本的制备将单独讨论。BAL的部位可能以胸部HRCT的检查结果为依据进行选择,应选择有影像学受累证据的区域。或者,对于弥漫性疾病,右中叶或舌叶是最常进行灌洗的位置,以最佳回收灌洗液。在为数不多的COP患者中已有关于BAL结果的报道。COP患者中的BAL液回收率比健康志愿者更低,但回收液中的细胞总数更大。COP患者中典型的BAL表现包括:淋巴细胞增多(20%-40%)、中性粒细胞增多(5%-10%)和嗜酸性粒细胞增多(5%-25%),淋巴细胞的量高于嗜酸性粒细胞。虽然不能借此诊断COP,但这种多种细胞增多的“混合模式”被认为具有特征性。COP患者的淋巴细胞计数往往高于特发性肺纤维化患者,但与过敏性肺炎相似。COP患者中可见的其他(非诊断性)BAL异常包括泡沫状巨噬细胞、肥大细胞、浆细胞、CD4/CD8 T细胞比率降低、基于HLA-DR或IL-2受体表达的活化T淋巴细胞增加。调查性研究已报道,Th1相关细胞因子水平增加,包括干扰素(interferon, IFN)-γ、IL-12和IL-18,但这些测试尚未用于临床。经支气管肺活检—对疑似COP患者开展经支气管活检的主要作用是识别鉴别诊断范畴中的其他疾病,因为经支气管肺活检标本量小,常常不足以最终证实COP和排除其他伴发疾病。OP的组织学特征在其他间质性肺疾病中可作为次要表现,所以依靠小的经支气管活检标本会增加遗漏核心诊断的可能性。另一方面,一些指南建议,对于有典型临床和放射影像学特征的患者,可以依据经支气管活检结果进行诊断。经支气管肺活检位置的选择主要根据胸部HRCT的检查结果,选择有放射影像学受累证据的区域。经支气管活检标本送检组织病理学分析和微生物学染色与培养。在适当的临床情况下,CT引导下肺活检可获得OP的组织学特征,从而减少外科肺活检的需求[。外科肺活检—通常需要进行开胸肺活检或胸腔镜肺活检以获得充足的肺组织标本(如,在肺膨胀时,最大直径>4cm)来明确诊断。肺活检位置的选择通常根据HRCT扫描发现的异常区域以及外科入路到这些区域的可行性。标本送检组织病理学和微生物学分析。除了充足的组织标本,重要的是给予病理科医生足够的临床信息,以指导其搜寻支持诊断的特异性病变和病理模式。诊断隐源性机化性肺炎—在缺乏促进因素或疾病过程的情况下,对于存在相符的临床和放射影像学表现的患者,COP的诊断依赖证实存在典型的组织病理学特征。在做出COP的组织病理学诊断时,必须满足两个关键条件:●存在OP的特征性组织病理学表现,包括主要位于小气道、肺泡管和邻近肺泡的管腔内炎性碎片栓,以及周围肺组织轻度间质性炎症。炎性碎片栓的成分为肉芽组织,其中包括埋入结缔组织基质的成纤维细胞和肌成纤维细胞。●没有提示其他疾病的组织病理学特征,例如:成形不良的肉芽肿提示过敏性肺炎,显著的嗜酸性粒细胞增多提示CEP,病变的时相异质性和成纤维细胞灶性分布提示寻常型间质性肺炎。为了有足够的组织标本供病理科医生排除其他疾病,如非特异性间质性肺炎或寻常型间质性肺炎,我们倾向于通过电视胸腔镜手术(video-assisted thoracoscopic surgery, VATS)或开胸手术获得肺活检标本,而不是经支气管肺活检。排除机化性肺炎的其他病因—当通过肺活检得出OP的诊断时,下一步是确定疾病是隐源性的还是继发于其他疾病。不可能根据放射影像学或病理学表现来鉴别COP与继发性OP。因此,需仔细回顾患者的病史、体格检查、用药情况、可能的暴露史和基础疾病,来确定COP是否确实为隐源性。鉴别诊断—COP的鉴别诊断包括一系列有着相似的临床特点、放射影像学表现、组织病理学表现或重叠的组织病理学特征的疾病。●社区获得性肺炎–COP的症状发作和放射影像学表现经常与社区获得性肺炎相似,但症状持续且对抗生素无反应提示COP,而非细菌性或病毒性肺炎。由于某些感染可能引起OP,所以阳性培养结果不一定能排除该诊断。●IIP–COP是IIP的一种类型,其他IIP类型是COP的鉴别诊断。有时,在另一种IIP的更为广泛的病理外观中可见小面积(<10%)的OP,如非特异性间质性肺炎或特发性肺纤维化。需要结合临床与病理来做出正确诊断。●过敏性肺炎–COP的临床表现类似于亚急性过敏性肺炎(咳嗽、呼吸困难、乏力、厌食及体重减轻)。在部分COP患者中也可见到亚急性过敏性肺炎的典型放射影像学表现(如,弥漫性微小结节、磨玻璃影)。已知暴露于病原体、BAL液中淋巴细胞百分比较高、肺活检发现成形不良的肉芽肿,均支持过敏性肺炎的诊断。然而,在过敏性肺炎中可见小面积的OP,所以这些疾病的鉴别需要临床结合病理。●肉芽肿性机化性肺炎-肉芽肿性机化性肺炎(granulomatous organizing pneumonia, GOP)是一种新描述的COP变异型,特征为OP的组织病理学模式与成形不良的非坏死性小肉芽肿密切相关。这些非坏死性肉芽肿必定局限在相同的细支气管周部位,并且位于OP模式区域内。该模式的原因不明,但被认为是一种变态反应或免疫反应。●CEP–CEP与COP可以有类似的临床表现,两种疾病的放射影像学均可见胸膜下斑片状实变区域。此外,可能观察到OP和嗜酸性粒细胞性肺炎共存的特征,表明部分患者可能从CEP转变为COP。这些疾病的鉴别通常取决于各种组织病理学模式所占的相对比例,以及对全身用糖皮质激素的反应。COP对治疗的反应一般较慢,从几日到1周不等,而CEP通常反应较快(几小时到几日)。●肺淋巴瘤–肺淋巴瘤的放射影像学表现可能与COP相似,呈斑片状、结节状实变区域和支气管充气征。单个实变区更常见于淋巴瘤而非COP,但也可见局灶性COP。这两种疾病可通过组织病理学和免疫组织化学表现加以鉴别。肺淋巴瘤样肉芽肿(pulmonary lymphomatoid granulomatosis, PLG)是一种淋巴细胞增生性疾病,为COP和肺淋巴瘤的鉴别诊断。在PLG中,胸部CT通常可见多个不明确的结节影,肺活检可见以下三联征:多形性淋巴样细胞浸润、动脉和静脉可见淋巴样细胞透壁性浸润(“血管炎”)以及在淋巴样细胞浸润区内存在局灶性坏死区域。●弥漫性肺泡损伤–弥漫性肺泡损伤(diffuse alveolar damage, DAD)是一种对肺损伤的非特异性组织病理学反应,最常见于急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)患者。偶有COP病例暴发性起病并迅速发展为呼吸衰竭。在这些患者中,COP为主要的病理模式,但也可见DAD区域。相反,在其他原因(例如,急性间质性肺炎)所致ARDS的增生期获取的肺活检标本中可见OP成分。需要仔细审查组织病理学表现以区分这些病变。 (●急性纤维素性机化性肺炎–急性纤维素性机化性肺炎(acute fibrinous and organizing pneumonia, AFOP)具有急性肺损伤的临床特征,可为特发性的或与其他病变相关,例如过敏性肺炎、感染、药物毒性、嗜酸性粒细胞性肺炎及风湿性疾病。组织病理学特征为肺泡内纤维蛋白沉积(纤维蛋白球)伴OP,但没有透明膜形成。对于肺活检显示多灶性纤维蛋白沉积或AFOP的患者,其OP复发率高于不存在纤维蛋白沉积或存在局灶性纤维蛋白沉积的患者(60% vs 6%,P<0.05)。治疗—尚无随机试验研究COP的治疗,因此治疗决策以实践指南、病例系列研究的观察结果以及我们的临床经验为依据。启动治疗的决策和初始治疗的选择取决于就诊时症状和肺功能受损的严重程度、病变的放射影像学范围以及疾病进展速度。病情轻且稳定—对于症状轻微的患者,若肺功能测定结果接近正常或正常并且仅为轻度的放射影像学受累,则在症状或肺功能出现任何恶化之前只进行监测而不给予治疗是合理的。此类轻度疾病患者偶尔可能自行缓解。每8-12周对患者重新评估,以了解症状或肺功能是否恶化。对于轻度至中度疾病患者,可以选择大环内酯类进行治疗,特别是对于期望避免糖皮质激素治疗的患者。少数病例报告称症状轻微的患者使用大环内酯类抗生素后有效,例如克拉霉素250-500mg,一日2次。在这些病例中,疗程需长至3-6个月;部分患者可以成功将大环内酯类抗生素的剂量减为一日1次,但过早停药常常导致疾病复发。大环内酯类的益处被认为与抗炎作用而非抗微生物作用有关。然而,COP的诊断经常是在患者应用1个或多个疗程的大环内酯类抗生素治疗假定的社区获得性肺炎失败后建立的,在这种情况下,大环内酯类抗生素治疗可能不够。病情持续或逐渐加重—大多数COP患者存在持续性的、令人困扰的和进行性的症状,伴中度肺功能受损和弥漫性放射影像学改变。对于这些患者,我们建议初始治疗予以口服糖皮质激素,通常可快速改善病情。在12项共纳入160例患者的研究中,60%的患者经泼尼松治疗后完全缓解,27%部分缓解,14%无效,6%为致死性结局。全身用糖皮质激素治疗的最佳初始剂量尚未知。我们遵循英国胸科学会指南的建议,通常使用的泼尼松初始剂量为0.75-1mg/(kg·d),且采用理想体重进行计算,最大剂量为100mg/d,早上单次口服。在我们的实践中,大多数患者的初始剂量为60mg/d。我们建议维持初始口服剂量4-8周。如果患者病情稳定或改善,在随后的4-6周,泼尼松逐渐减量至0.5-0.75mg/(kg·d),同样使用理想体重进行计算。经过3-6个月的口服泼尼松治疗后,如果患者病情仍然稳定或改善,激素可逐渐减量至停药。只要仍需要全身用糖皮质激素治疗,除了临床评估外,还需要每2-3个月对患者随访常规胸片和肺功能检查。出现疾病加重或复发的首个迹象时,泼尼松剂量应增加至之前的剂量或立即重新开始。值得注意的是,在患者出现显著症状之前胸片表现就可能发生改变。停用糖皮质激素之后,我们会在接下来的一年对患者进行临床随访,并且大约每3个月复查一次胸片。糖皮质激素治疗会产生多种副作用。因此,需要仔细和持续评估风险和获益。最大程度减少全身用糖皮质激素不良反应(例如,感染、骨质疏松、肌病及肾上腺抑制)的步骤将单独讨论。全身使用糖皮质激素治疗无效—对病情稳定,但全身应用糖皮质激素仍无改善的患者,我们回顾最初的诊断性检测结果以确保没有误诊、漏诊。也应排除继发感染,尤其是如果病情最初改善后出现恶化。这种情况下,常常需要复查支气管镜加BAL。●细胞毒疗法再次确认COP的诊断后,在维持口服泼尼松治疗的同时,通常开始应用细胞毒药物。我们通常使用环磷酰胺,虽然支持这种选择的数据仅限于病例报告。对于肾功能正常的患者,初始剂量为1-2mg/(kg·d),一日1次,最大剂量为150mg/d,但治疗COP的最佳剂量尚未知。我们通常以50mg/d开始给药,在2-4周内缓慢增加剂量。对于肾功能异常的患者,需要调整环磷酰胺的剂量,或使用其他药物。为确保有足够的机会以获得临床疗效,至少需要尝试3个月。由于环磷酰胺的毒性,我们在6个月后停用该药。环磷酰胺的潜在不良反应和安全用药指导将单独讨论。●其他疗法有病例报告显示,在全身用糖皮质激素的基础上加用大环内酯类抗生素有益。一项病例系列研究显示,4例停用糖皮质激素之后疾病复发的患者采用大环内酯类药物取得成功治疗,且没有明显的不良反应。一篇文献综述建议,大环内酯类药物应该用作其他治疗(如糖皮质激素)的辅助治疗。 在少数病例报告中,已有人使用环孢素联合糖皮质激素治疗快速进展性COP。一项病例系列研究描述了4例患者对糖皮质激素治疗没有反应,但加用利妥昔单抗后获得了至少部分改善;一例患者获得完全缓解。不能逐渐减量糖皮质激素或不能耐受激素的不良反应—COP复发很常见,通常发生在糖皮质激素治疗1-3个月后逐渐减量时。在一些病例系列研究中,超过1/2的患者在其病程中至少经历了1次临床复发。大多数这些患者重新应用糖皮质激素治疗后将会改善,复发似乎一般不会影响整体长期预后。病情持续或频繁复发(>3次)的患者,可能需要长期的泼尼松和糖皮质激素助减剂治疗。对于糖皮质激素治疗有效但需要高剂量才能控制病情的患者,以及不能耐受糖皮质激素不良反应的患者,我们通常将硫唑嘌呤作为糖皮质激素助减剂。不过,支持糖皮质激素助减剂用于COP的资料有限。少数病例报告描述了联用硫唑嘌呤和低剂量泼尼松的有利结局。硫唑嘌呤的毒性作用部分与硫代嘌呤甲基转移酶(thiopurine methyltransferase, TPMT)缺乏有关,使用硫唑嘌呤之前分析TPMT基因可能有助于预测那些有严重中毒风险的个体。硫唑嘌呤的药理学和不良反应将单独讨论。暴发性疾病—根据临床经验和病例报告,对于少数病情进展迅速和病变广泛的患者(例如,需要高流量辅助供氧),在排除感染后,我们建议静脉用糖皮质激素作为初始治疗,例如甲泼尼龙125-250mg,每6小时1次,或750-1000mg静脉冲击,一日1次,持续3-5日。一旦患者表现出改善迹象(通常在5日内),糖皮质激素治疗可改为口服泼尼松0.75-1mg/(kg·d),使用理想体重进行计算,最大剂量为100mg/d。后续的糖皮质激素减量以及激素长期不良反应的预防已在上文介绍。对于需要机械通气治疗呼吸衰竭的患者,或对于静脉给予糖皮质激素没有快速反应的患者,目前尚不清楚是否该加另一种免疫抑制剂,但我们通常会加。我们通常选用环磷酰胺,因为其应用经验更丰富。6个月后应停用环磷酰胺,如果患者有不良反应则应更早停用。一份病例报告介绍了静脉用甲泼尼龙联合口服吗替麦考酚酯,但目前尚不清楚吗替麦考酚酯是否促进了暴发性OP的消退。局灶性机化性肺炎—对于大多数患者,作为初始治疗,切除含局灶性OP的孤立肺结节就已足够了。2项回顾性研究发现,在共计43例患者中,在切除的孤立性肺结节中发现了局灶性OP。对于这些患者没有给予进一步的治疗,其中41例患者未见复发,2例局部复发的患者经糖皮质激素成功治疗。随后一项报告进一步支持单独手术切除就足以治疗局灶性OP。预后—2/3的患者经糖皮质激素治疗后康复,通常表现为临床和生理完全改善,胸片显示正常。症状的改善偶尔十分显著,出现在1-2周时,而大多数患者是在数周至数月内更为逐渐的改善。尽管临床改善,系列HRCT扫描可能显示异常持续存在。胸片显示气腔高密度影的患者比显示网状阴影的患者结局要好得多。约1/3的患者会存在持续性症状、肺功能测定结果异常以及放射影像学病变。通常,就诊时疾病的严重程度与之后复发的可能性相关,例如低氧血症的严重程度、放射影像学异常的范围、肺功能下降的严重程度、存在基础疾病或者治疗延迟的时间长度。COP的总体预后比其他间质性肺疾病要好得多,其他疾病例如特发性肺纤维化、纤维化非特异性间质性肺炎以及急性间质性肺炎。罕见快速致命性COP。总结与推荐临床表现和诊断●隐源性机化性肺炎(COP)是特发性间质性肺炎的一种。●当机化性肺炎(OP)与其他病理过程(如,结缔组织病、多种药物、恶性肿瘤或其他间质性肺炎)有关时,称为继发性OP。●COP发病通常是在40-49岁或50-59岁,受累的男女患者数量相当。大多数患者的症状持续不到2个月,临床表现类似于社区获得性肺炎(如,咳嗽、劳力性呼吸困难及体重减轻)。约一半患者起病前有流感样疾病。●COP最常见的胸部影像学特征是多发性磨玻璃影或实变影。肺功能测定通常显示限制性通气障碍伴气体交换缺陷。●可屈性支气管镜常用于获取支气管肺泡灌洗液(BAL)标本以评估感染、出血和恶性肿瘤。在该操作期间有时取活检组织用于组织病理学和微生物学检查。但是,对于明确COP的诊断,外科肺活检(胸腔镜或开胸肺活检)一般优于经支气管肺活检。●COP的特征性组织病理学表现包括肉芽组织在肺泡管和肺泡内过度增生或形成“栓子”,伴有周围肺泡的慢性炎症。●COP的诊断需要通过组织病理学发现OP这一主要病理模式并排除任何可能的其他病因,这些病因可能相对明显,也可能需要艰辛的搜查。此外,COP的鉴别诊断包括多种疾病,需要加以排除。治疗●对于COP,启动初始治疗的决定和初始治疗的选择取决于就诊时症状和肺功能受损的严重程度、病变的放射影像学范围以及疾病进展速度。●对于症状轻微的COP患者,若肺功能测定结果无异常或仅有轻度异常,在症状或肺功能出现任何恶化之前只进行监测而不给予治疗是合理的做法。每8-12周对患者重新评估:症状是否加重、肺功能是否恶化或放射影像学上的阴影是否进展。●对于COP所致中度或更严重呼吸功能受损的症状性患者,我们推荐启动全身性糖皮质激素治疗(Grade 1B)。常用剂量为泼尼松0.75-1mg/(kg·d)的等效剂量,使用理想体重进行计算,最大剂量为100mg/d,早晨单剂口服;大多数患者使用60mg/d的剂量有效。●对于疾病快速进展或发生呼吸衰竭/即将发生呼吸衰竭的患者,我们建议初始给予大剂量糖皮质激素治疗(甲泼尼龙500-1000mg/d,静脉给药,持续3-5日),而不是较小的口服剂量。●对于全身用糖皮质激素初始治疗无效的患者或疾病呈暴发性的患者,我们建议加用另一种免疫抑制剂,如环磷酰胺或硫唑嘌呤)。●糖皮质激素治疗数日至数周后,通常可实现临床改善及胸部影像学检查所见阴影消失。口服糖皮质激素根据患者的耐受情况在6-12个月内逐渐减量。在糖皮质激素停药或减量后常见复发,常常导致治疗时间延长。●对于不能将激素逐渐减量到不会引起不可耐受的不良反应的水平的患者,我们建议加用另一种免疫抑制剂,如硫唑嘌呤。●糖皮质激素治疗可能导致多种副作用。最大程度减少全身用糖皮质激素不良反应(例如,感染、骨质疏松、肌病及肾上腺抑制)的步骤将单独讨论。
张永明 副主任医师 中日医院 呼吸与危重症医学科1.5万人已读 - 医学科普 结节病的病因、发病机制、临床表现、诊断、治疗最新研究进展
结节病是多系统受累的肉芽肿性疾病,病因不明,全世界范围内均有发病,病理特征是受累脏器存在非干酪样肉芽肿。通常影响年轻成人,最初表现为以下异常中的1项或多项:●双侧肺门淋巴结肿大●肺部网状影●皮肤、关节和/或眼部病变流行病学——结节病的患病率(估计为10-20/100,000人)和年发病率尚不确切。该病发病率似乎有地区差异,也表现出家族和特定族群的聚集现象,黑人中更常见(是白人的3-4倍。据估计,美国黑人患结节病的终生风险是2.4%,而白人为0.85%。一项单中心病历回顾研究纳入的队列包含明尼苏达州奥姆斯特郡居民,1976-2013年确定了448例结节病新发病例,或者说约每年10人/100,000。女性发病高峰年龄从1950年的40-59岁变为2010年的50-69岁。男性发病高峰年龄从1950年的30-49岁变为2010年的40-59岁。97%的患者有胸内受累证据,但仅43%的患者有呼吸系统症状。这些患者中90%以上为白人。来自此队列的数据证实女性发生结节病时年龄通常更大。此外,有结节病患者的住院率高于无结节病患者(RR 1.37,95%CI 1.24–1.52),尤其在患有结节病的女性中。此外,患者的免疫遗传背景可能在结节病的临床表现中发挥作用,并且可能是构成该病异质性的基础。流行病学研究显示,疾病表现和严重程度在不同种族族群间存在显著异质性。例如,与白人相比,黑人通常发病更急、病情更严重,而白人多无症状且呈慢性病程。病因—尽管大量研究,但结节病确切的病因和发病机制仍未知。一个普遍接受的假说认为,结节病有多种病因,疾病的不同模式可能部分程度上与不同的基础病因有关。临床表现青少年与成人——结节病通常出现在20-60岁的患者中,黑人发病比白人早约10年=。在约一半的病例中,其结节病是在症状出现前、行常规胸片显示放射影像学异常(如双侧肺门淋巴结肿大、网状影等)而偶然检出。=结节病最常累及肺部,但最高达30%的患者表现出结节病的胸外表现=。肺受累的典型表现是弥漫性间质性肺疾病,其他较少见的肺部表现包括气胸、胸膜增厚、乳糜胸和肺高压。结节病的肺外表现将单独介绍。=常见的呼吸道主诉症状包括咳嗽、呼吸困难和胸痛,并常伴有乏力、不适、发热和体重减轻=。70岁以上患者似乎更可能出现全身症状,如乏力和厌食;然而,呼吸困难和咳嗽一般同时存在=。全身炎症可能促进肌肉无力和运动不耐受=。应询问患者有无新发皮肤病变(特别是纹身或瘢痕周围)、视力改变、干眼或口干、腮腺肿胀、心悸、晕厥、关节疼痛或肿胀,或者肌肉无力。即使存在肺实质的结节病,胸部检查时也不常听到湿啰音。存在支气管内受累或瘢痕所致牵引性支气管扩张时,可能出现哮鸣音。杵状指(趾)罕见,通常与晚期肺纤维化有关。肺外结节病的体格检查结果将单独讨论。儿童——症状性结节病在儿童中较罕见。与白人儿童或亚裔儿童相比,非裔儿童的病情更重且病变更广泛。8-15岁儿童可发生多系统受累,与在成人中的发现类似。较年幼的儿童常表现为皮疹、关节炎和葡萄膜炎,而无明显肺部受累。在非裔美国儿童中,淋巴结受累、高球蛋白血症和高钙血症的发病率趋于更高。一项关于丹麦结节病儿童的病例系列研究显示,最常见的首发症状为结节性红斑(erythema nodosum,EN)和虹膜睫状体炎。90%的患儿有胸片异常。评估——应对所有疑似结节病患者进行全面的初始评估。初始评估的目的包括:获得更多资料来支持结节病的诊断、同时排除其他诊断,明确肺部受累严重程度,并识别可能适合活检或需立即治疗的肺外器官受累。建议的评估内容包括以下:●病史,包括职业和环境暴露●全面的体格检查●实验室检查●结核菌素皮肤试验●后前位胸片,以及常用高分辨率计算机断层扫描(high resolution computed tomography,HRCT)●肺功能测定(pulmonary function tests,PFTs)●心电图●眼科检查实验室检查——实验室检查通常包括全血细胞计数和分类计数、肝功能检查、血尿素氮、肌酐、血糖、电解质、血清钙和尿液分析[27]。在对患者进行结节病评估时,我们通常行HIV感染的血清学检测。红细胞沉降率和C反应蛋白(c-reactive protein,CRP)是炎症的非特异性指标,是否作此类检测并无统一性。血清血管紧张素转化酶(angiotensin converting enzyme,ACE)水平和Kveim试验的临床应用有限,将在下文介绍。结节病患者可能有多种实验室检查异常:●贫血并不常见。如有贫血,通常起因于慢性疾病的贫血,但是某些患者可出现脾功能亢进、骨髓受累或自身免疫性溶血性贫血。●可见白细胞减少(5%-10%)、嗜酸性粒细胞增多(3%)[和血小板减少(罕见)。●红细胞沉降率常升高,但无助于评价疾病活动度。●约1/3的结节病患者CRP轻度升高,但其不能区分结节病和其他原因所致炎症,在结节病患者中其只与乏力有关且不一致。CRP与治疗反应之间的关系还在研究中。●高钙尿症较高钙血症更为常见。●血清碱性磷酸酶浓度中等程度升高提示弥漫性肉芽肿性肝脏受累。●可出现高丙种球蛋白血症(30%-80%)和类风湿因子阳性,但不经常进行这些检查。血清标志物——已研究了一些血清学标志物在诊断或监测疾病活动度当中的潜在作用,例如血清ACE、腺苷脱氨酶(adenosine deaminase,ADA)、血清淀粉样蛋白A(serum amyloid A,SAA)和可溶性IL-2受体,但没有其效用的确切证据。在未经治疗的结节病患者中,有75%出现血清ACE水平升高。然而,由于敏感性低(假阴性结果)和特异性不足(近10%的假阳性率),血清ACE作为诊断性检查的应用价值有限。可出现血清ACE水平升高的其他疾病过程。ACE的组织水平通常非常高,但该检查不在临床上应用。通过监测ACE水平来评估病程,这一方法的价值尚未明确。可能在结节病患者的血清和支气管肺泡灌洗(bronchoalveolar lavage,BAL)液中发现ADA水平升高。然而,考虑到敏感性和特异性低,ADA的临床应用有限。还发现结节病患者的SAA升高,但也尚未证实此检测在临床上有用。有学者提出血清可溶性白细胞介素-2受体(serum soluble interleukin-2 receptor,sIL2R)可作为确定结节病患者肺外受累的有用标志物。Kveim试验——Kveim试验以结节病患者经加热灭菌的脾细胞悬液(Kveim-Siltzbach试剂)进行皮内试验(与结核菌素皮肤试验类似),经约3周的时间,诱发出结节病肉芽肿性反应。由于试验所用试剂的普及程度有限以及担心试验中出现疾病传播,Kveim试验基本上只是研究工具。结核病检测——除非已充分证明患者的结核菌素皮肤试验为阳性,否则应对患者进行结核菌素皮肤试验或γ干扰素释放试验,以帮助排除结核分枝杆菌感染。预计结节病患者的皮肤试验反应性应该减弱,因此若试验结果阳性,则是有力支持分枝杆菌疾病的证据。肺部影像学检查——90%以上的结节病患者存在肺部受累。肺部影像学检查在结节病的诊断中发挥着不可或缺的作用,首先拍摄胸片,通常随后行HRCT。其他影像学检查用于特定指征,如18F-FDG-PET、镓-67、铊-201和司他比锝(MIBI-Tc)单光子发射计算机断层扫描(single photon emission computed tomography,SPECT),将在下文介绍。胸片——因疑诊结节病而接受评估的所有患者均应行胸片检查。双侧肺门淋巴结肿大是结节病的典型表现,肺门可能对称性增大(在约50%的病例中)或右侧稍更显著。真正的单侧淋巴结肿大并不常见(<5%的病例)。肺实质表现更为多样,可为正常、弥漫性网状影或磨玻璃样不透光区、结节性实变或囊性瘢痕形成。现已根据胸部X线摄影表现对肺部受累进行分期,尽管这能提示肺部受累的解剖学情况,但并不能反映疾病活动度或功能受损程度。X线摄影表现分期如下:●Ⅰ期–Ⅰ期定义为存在双侧肺门淋巴结肿大,常伴有右气管旁淋巴结肿大。受累患者中有50%其结节病最初表现为双侧肺门淋巴结肿大。这类患者中有75%其肺门淋巴结肿大在1-3年内消退,而有10%进展为慢性肺门淋巴结肿大、可持续10年或以上。当双侧肺门淋巴结肿大伴有结节性红斑(EN)、游走性多关节痛和发热时,诊断极可能为Lofgren综合征。●Ⅱ期–Ⅱ期定义为双侧肺门淋巴结肿大和网状阴影(相较于下肺野,网状影更常出现在上肺野)。25%的患者在最初诊断时存在这些表现。这类患者中有2/3会自发缓解,而其余患者随时间推移病情进展或出现微小变化。Ⅱ期疾病患者通常有轻至中度症状,最常见为咳嗽、呼吸困难、发热和/或易疲劳。●Ⅲ期–Ⅲ期表现为网状阴影,伴肺门淋巴结缩小。网状影主要分布于上肺野。●Ⅳ期–Ⅳ期疾病的特征为网状影伴肺容积损失的证据,这些主要分布在上肺野。可能还会观察到融合肿块伴显著的牵引性支气管扩张。还可见广泛钙化以及空洞或囊腔形成。较不常见情况下,胸片可显示多发双肺结节和极轻度的肺门淋巴结肿大,这些表现可能酷似转移性疾病。结节病病程较长时,肺门或纵隔淋巴结钙化的情况更常见;这种表现不具特异性。胸膜受累不常见(<5%的患者),但可造成淋巴细胞性渗出性胸腔积液、乳糜胸、血胸和气胸。HRCT扫描—常进行胸部HRCT以评估胸片所见异常,或者评估胸片正常患者原因不明的呼吸困难或咳嗽。HRCT可发现胸部X线平片未能发现的肺实质和纵隔异常:●肺门和纵隔淋巴结肿大●支气管血管束串珠样增厚或不规则增厚●沿支气管、血管及胸膜下区域分布的结节●支气管壁增厚●磨玻璃样不透明影●肺实质肿块或结节性实变,偶伴有空洞●肺实质条索●囊腔●纤维化伴肺结构变形和牵引性支气管扩张HRCT扫描通常显示肺实质变化主要分布于中上肺野。一项小型病例系列研究评估了HRCT发现与组织学异常的相关性,发现磨玻璃样不透光区与结节病肉芽肿相关、而非肺泡炎。尽管可发生淋巴细胞性肺泡炎,但在具有临床意义的结节病患者中很少发现该病变。FDG-PET扫描—尚不明确18F-FDG-PET在结节病评估中的作用。它可能有助于发现比肺部病变更适合活检的隐匿病变[。该检查不能区分恶性肿瘤和结节病,因为两种疾病的18F-FDG-PET扫描结果均可为阳性。在未来,使用其他示踪剂可能提高PET显像在结节病诊断中的效用。在一项小型研究中(24例结节病、17例肺癌),联合18F-FDG和18F-甲基酪氨酸(methyltyrosine,18F-FMT)PET扫描能够区分结节病与恶性肿瘤;结节性病变在18F-FDG-PET扫描中为阳性、但在18F-FMT-PET扫描中为阴性(癌症患者的2种扫描结果均为阳性)。尚需开展更多研究来确认。可能并非所有机构都有18F-FMT示踪剂。FDG-PET扫描还可能有助于评估心脏结节病,作为对MRI的补充。其他放射性示踪剂扫描—镓-67是放射性示踪剂,聚集于炎性病灶中,但几乎不被正常肺组织摄取。并不推荐使用镓-67常规评估结节病,因为阴性扫描结果并不能排除结节病,而且肺摄取增多对于结节病也并无特异性。镓扫描所见“熊猫征”和“λ征”的联合表现偶尔有助于诊断结节病。在所有病变部位都不适合活检的这种不常见情况下,使用该检查来为结节病的诊断提供依据。在鼻咽部黏膜正常摄取镓的基础上,加上双侧泪腺和腮腺摄取镓,即形成“熊猫征”。右侧气管旁和双侧肺门淋巴结对镓的摄取,因此扫描结果与希腊字母“λ”相似,称为“λ”征。认为同时出现这两种征象是支持诊断结节病的强有力证据,不过单独的熊猫征可见于干燥综合征。在未来,基于放射性示踪剂的其他类型扫描可能有助于对结节病患者的诊断和临床评估。例如,在疑似心肌结节病患者的评估中,有时应用铊-201显像和司他比锝(MIBI-Tc)SPECT,但是通常优选MRI和FDG-PET。生长抑素受体在恶性肿瘤和炎性疾病中过度表达,锝标记的地普奥肽(depreotide)会与这种受体结合。一项评估锝标记地普奥肽扫描的初步试验扫描了22例已知存在结节病的患者。18例(81%)患者的扫描结果为阳性,而另外4例全身扫描结果为阴性的患者胸部X线平片均正常,他们先前自诊断后存在的异常已消失。目前仍不明确这种检查的完整工作特性,其临床应用仍处于实验阶段。肺功能测定—对肺结节病患者行肺功能测定(PFTs),包括肺量计检查、肺容积、肺一氧化碳弥散量(diffusing capacity for carbon monoxide,DLCO)和6分钟步行试验(six minute walk test,6MWT),以评估患者呼吸系统受损的严重程度,并通过连续测定以监测病程。PFTs并不能可靠地检出肺实质结节病(HRCT更佳),也不能准确估计实质病变的范围/程度。此外,临床医生仅根据PTFs不能预测肺部受累的自然病程或治疗效果。约20%的Ⅰ期结节病患者PFTs结果为异常。相比之下,40%-70%的Ⅱ-Ⅳ期结节病患者PFTs异常。特征性的PFTs结果会提示限制性模式(肺活量和肺总量下降)伴DLCO下降,但是肺功能正常并不少见。支气管内结节病可造成气流受限及阻塞性呼吸生理学改变。大部分结节病患者6MWT距离缩短,这与用力肺活量及动态脉搏血氧饱和度下降相关。人们认为6MWT提供了结节病的综合评估,因其受肺外因素的影响,例如肌力、乏力和心功能。动脉血气可能正常,也可能显示低氧血症和低碳酸血症(过度通气)。运动可能使这些异常更明显。动脉血气检查的主要指征是评估有无高碳酸血症,因为氧合情况通常是通过静息和劳力状态下的脉搏血氧饱和度来评估。诊断诊断方法—针对结节病,没有确定性诊断性检查。但结节病的诊断需要3要素:●临床和X线摄影表现符合结节病●排除可能表现相似的其他疾病●组织病理学检查发现非干酪样肉芽肿对疑似结节病的所有患者进行综合评估满足上述要素后,对大多数病例实施诊断性操作。一般而言,诊断为结节病需要1个以上器官系统受累,但是并非总是需要对另一个部位也行活检。例如,一个器官(如皮肤、肺)有非干酪样肉芽肿,结合结节病另一个器官系统的临床证据(如高钙血症、双侧肺门增大),一般足以做出结节病的诊断。无需活检的主要情况包括:无症状患者存在双侧肺门淋巴结肿大(Ⅰ期),可在无活检的情况下受到监测;出现典型Lofgren综合征症状(发热、EN、关节痛和双侧肺门淋巴结肿大)的患者。对于后面这种患者,如不能用其他疾病来解释存在的这一系列表现,并且如果异常自发迅速消退,通常不需要活检。值得注意的是,不应对EN病变进行活检,因为即使存在结节病,该病变的组织病理学检查也将显示脂膜炎、而非肉芽肿。活检部位的选择—应对看上去受累、最容易获取的组织进行活检,这可能包括皮肤病变、皮下结节、可触及的淋巴结、肿大的腮腺、结膜病变、增大的泪腺或某些其他眼部病变。若患者看上去并不存在上述任何部位受累,则下一步选择通常是对X线摄影显示的肿大胸内淋巴结或肺实质进行活检或细针抽吸活检。部分患者有确定存在于肺外部位的非干酪样肉芽肿,但仍需进行支气管镜检查,例如患者存在提示感染的全身症状或具有不典型临床及影像学表现。例如,对于存在空洞性肺部病变的患者,在启动任何免疫抑制治疗前,可能需行支气管镜检查以排除分枝杆菌和真菌感染。同样,对于不典型纵隔淋巴结肿大患者,通常需行纵隔淋巴结取样。对于存在肺实质病变、但无明显纵隔淋巴结肿大或肺外病变(经仔细检查后)的患者,选择经支气管肺活检还是胸腔镜肺活检,取决于对结节病的怀疑程度。因为经支气管肺活检对结节病的检出率高,所以对于强烈怀疑其为结节病的患者(如,HRCT显示支气管血管束串珠样改变的年轻患者),适合选择这种活检方法。相反,对于结节病可能性较小,而更可能为其他诊断且诊断需要较大样本的患者,优选胸腔镜肺活检。支气管镜检查—在纤维支气管镜下进行支气管肺泡灌洗(BAL)、支气管内活检和经支气管活检是诊断结节病的微创传统方法。●BAL–BAL可用作一种辅助方式,通过显示以下结果而支持结节病诊断:CD8细胞数量减少,CD4/CD8比值增高,及活化T细胞、CD4细胞、免疫球蛋白和IgG分泌细胞数量的增加。BAL也用于排除其他诊断,如感染和恶性肿瘤。灌洗液中发现淋巴细胞增多对于结节病的诊断既无特异性、也无敏感性。因此该发现有可能误导诊断。例如,一项研究评估了128例各种原因引起BAL淋巴细胞增多的未经治疗患者。尽管该研究存在局限性,但有几项结果尤其值得关注:对结节病最具特异性的检查是发现以下三联征:CD4/CD8比值>4:1、淋巴细胞百分比≥16%,以及经支气管活检显示非干酪样肉芽肿。这些发现联合起来区分结节病与其他间质性肺疾病的阳性预测值(positive predictive value,PPV)为100%,区分结节病与所有其他疾病的PPV为81%。CD4/CD8比值<1对结节病的阴性预测值达100%。然而,鉴于有以CD8为主的结节病病例报道,因此应谨慎解读该结果。BAL液的中性粒细胞>2%或嗜酸性粒细胞>1%提示结节病并非正确诊断。BAL液中发现D-二聚体也支持结节病的诊断,但这种方法主要是研究工具。一项观察性研究发现,10例结节病患者中有8例的BAL液中有可检测的D-二聚体(定义为每毫升浓缩BAL液中D-二聚体>78ng),而在18例健康对照者中均无此发现。在结节病患者中,黑人患者BAL液中存在D-二聚体的可能性似乎高于白人患者[。●支气管内和经支气管肺活检–支气管内和经支气管肺活检可使患者避免接受外科活检。所有进行纤维支气管镜检查的患者,均应观察气道寻找有无支气管内病变,例如红斑或者结节、颗粒或鹅卵石样外观。约40%的Ⅰ期结节病患者和约70%的Ⅱ期或Ⅲ期结节病患者存在支气管内病变。通常获取4-6块支气管内活检样本,最好选择黏膜发红部位,或者黏膜正常时选择一级和二级气管分叉处。对于结节病,支气管内黏膜活检通常是阳性的,与单纯行经支气管肺活检相比,可能增加诊断性检出率[72]。一项病例系列研究纳入37例结节病患者,支气管内活检的诊断性检出率为24%,比单纯经支气管肺活检的检出率增高了8%。对于根据双侧肺门淋巴结肿大或HRCT显示相符肺实质表现(如,沿支气管血管束串珠样或不规则增厚)而怀疑存在结节病的患者,经支气管肺活检的检出率相对较高(50%-75%)。获取的标本应既用于培养、又用于组织学染色,包括抗酸杆菌和真菌染色。●经支气管针吸活检–经支气管针吸活检(transbronchial needle aspiration,TBNA)可与经支气管肺活检在同一次操作期间采用同一支气管镜进行,以获取肺结节和纵隔淋巴结的细胞学样本或空芯针穿刺活检组织样本。或者,可在超声引导下行TBNA。如前所述,样本应送检进行病理学和微生物学检测。TBNA操作技术及其在结节病诊断中的作用将单独介绍。超声内镜引导下的针吸活检—对于纵隔淋巴结肿大且临床怀疑为结节病的患者,超声内镜引导[通过食管超声内镜(endoscopic ultrasound,EUS)或支气管内超声(endobronchial ultrasound,EBUS)]的胸腔内淋巴结针吸活检的诊断性检出率为80%-90%。选择这些操作中的哪一种,取决于现有专业技术和设备以及CT显示的胸腔内肿大淋巴结的位置。这些技术及其对结节病的诊断性检出率,将单独作更详细的讨论。纵隔和肺的外科活检—如果创伤较小的方法不能明确诊断,可能需要通过纵隔镜进行纵隔淋巴结活检,或者通过胸腔镜或开胸术进行肺活检。在双侧肺门淋巴结肿大以及胸片正常的患者中,有60%经纵隔镜淋巴结活检为阳性。有时,在患者仍处于麻醉状态时,通过冷冻切片检查纵隔淋巴结活检。如果淋巴结未发现肉芽肿,则应行胸腔镜下肺活检或开胸肺活检,但如果淋巴结显示非干酪样肉芽肿,对患者无需进行肺活检。然而,如果肺实质表现对结节病来说不典型,淋巴结活检和肺活检可能均需要。所有活检标本均应进行组织病理分析、针对分枝杆菌和真菌的特殊染色,以及分枝杆菌和真菌培养。组织病理学—结节病的特征性形态学表现是非干酪样肉芽肿。在肺部,最常发现肉芽肿存在于肺泡间隔、支气管壁,以及沿肺动脉和静脉分布。结节病肉芽肿形成之前可能有累及间质组织多于肺泡腔的肺泡炎,且其肺泡炎的特征是炎症细胞积聚(包括单核细胞、巨噬细胞和淋巴细胞)。结节病肉芽肿是局灶性、慢性炎症反应,由上皮细胞、单核细胞、淋巴细胞、巨噬细胞和成纤维细胞聚集而形成。肉芽肿中心的成熟上皮样细胞(称为“granuloma follicle”)间常发现多核巨细胞,多核巨细胞细胞质中常有包涵体,如星形小体、舒曼(Schaumann)小体和双折光结晶颗粒(草酸钙和其他钙盐)(。大多数结节病肉芽肿会逐渐消退,之前的炎症很少有遗留表现或没有。可能观察到少量中心区域纤维素样坏死,但大量坏死提示其他疾病或坏死性结节病样肉芽肿病。结节病样组织病理改变还可见于某些肿瘤性疾病患者的淋巴结,如霍奇金病和其他淋巴细胞增生性疾病、生殖细胞睾丸肿瘤、乳腺癌、肾细胞癌、平滑肌肉瘤和卵巢黏液囊腺瘤等等。因此,当患者淋巴结表现为结节病样肉芽肿、但无结节病其他典型特征时,建议需保持谨慎。鉴别诊断—结节病诊断的不可或缺步骤之一是排除其他可能,有几种情况特别难以诊断。例如,当不存在肺外表现、双侧肺门淋巴结肿大或纵隔淋巴结肿大时,诊断可能较为困难。同样地,存在HIV感染、潜在的职业或环境因素暴露史和/或显著的全身症状时,可能更难诊断。显著的全身症状(如,发热、盗汗、体重减轻和/或乏力)可增加对感染或恶性肿瘤的怀疑。对于疑似恶性肿瘤的患者,如淋巴结活检显示非干酪样肉芽肿,则需仔细检查以排除合并恶性肿瘤的可能。除结节病以外的其他肺部肉芽肿性疾病包括:●分枝杆菌感染–结节病和肉芽肿性肺部疾病要与结核和非典型分枝杆菌感染区分。因此,所有活检标本均应进行针对分枝杆菌的特殊染色并尽可能进行培养。●真菌感染–结节病需与真菌感染区分,如组织胞浆菌病、芽生菌病、耶氏肺孢子菌(Pneumocystis jirovecii)感染。因此,所有活检样本均应进行针对真菌的特殊染色并尽可能获取BAL液进行培养。在组织胞浆菌病流行区域,还应进行尿、血清和BAL液的抗原检测。●过敏性肺炎–如果遗漏了潜在抗原的暴露史,那么过敏性肺炎(hypersensitivity pneumonitis,HP;也称为外源性过敏性肺泡炎)可被误诊为结节病。详细的职业暴露史将有助于排除HP的很多原因。HP肉芽肿通常位于呼吸性或终末细支气管附近,而结节病肉芽肿位于支气管血管结构周围、具有沿淋巴结构分布的特点。与结节病肉芽肿相比,HP肉芽肿更小、没有那么分散,且伴有更严重的肺间质慢性炎症。●尘肺–某些尘肺(特别是慢性铍病)的影像学及病理学表现可与结节病类似。诊断慢性铍病应基于仔细询问职业史,并在必要时进行血铍淋巴细胞增殖试验。●药物诱导的超敏反应–据报道,有多种药物可导致有肉芽肿形成的药物诱导超敏反应,包括:甲氨蝶呤、依那西普、英夫利西单抗、阿达木单抗、阿扎胞苷、奥沙利铂、阿莫西林、西罗莫司、氟西汀和膀胱内给药的卡介苗(Bacillus Calmette-Guerin,BCG)[92-97]。●肺组织细胞疾病–肺朗格汉斯细胞组织细胞增生症(嗜酸性肉芽肿)和另一种组织细胞增殖性疾病Erdheim-Chester病,可造成上肺野炎症和瘢痕。根据活检结果来区分。染色时朗格汉斯细胞呈S-100和CD1a阳性。Erdheim-Chester病细胞表达组织细胞标志物CD68,但与朗格汉斯细胞组织细胞增多不同,不表达CD1a或S100。●异物肉芽肿–异物肉芽肿(foreign body granulomatosis,FBG)可由吸入或静脉注射异体物质所致。FBG的组织病理学典型表现为血管周围纤维化及聚集的多核巨细胞和肉芽肿。可极化物质可能出现于肉芽肿和巨细胞内,或者出现于细胞外的血管壁中。●血管炎症相关疾病–肉芽肿性多血管炎(Wegener肉芽肿)、嗜酸性肉芽肿性多血管炎(Churg-Strauss综合征)和肺淋巴瘤样肉芽肿病,这些疾病与结节病的区分点在于它们的血管中心性特点及伴有血管炎证据。血清抗中性粒细胞胞质抗体(antineutrophil cytoplasmic antibody,ANCA)检测可能有助于识别系统性血管炎。●支气管中心性肉芽肿病–支气管中心性肉芽肿病的特征为支气管周围和细支气管周围分布的坏死性肉芽肿性炎症。所有病例中约50%伴有哮喘和变应性支气管肺曲霉病。●原发性免疫缺陷–慢性肉芽肿病患者常对感染因子产生肉芽肿反应,但也可出现非感染性肺肉芽肿。普通变异型免疫缺陷病(common variable immunodeficiency,CVID)患者中可见结节病样病变,有肝脏和肺的肉芽肿浸润,常见不同程度的ACE水平增高。因此,看起来是结节病的患者如出现低丙种球蛋白血症及反复感染,应评估是否为CVID。这些疾病将单独讨论。●免疫重建炎症综合征–开始强效联合抗逆转录病毒治疗(antiretroviral therapy,ART)后数月如果发生结节病,提示免疫重建可能“触发”既存亚临床结节病再激活或出现。实际上,部分(但非所有)免疫重建炎症综合征(immune reconstitution inflammatory,syndrome,IRIS)相关结节病患者曾有已知的结节病史,其结节病数年前就已静止。疾病程度的初始评估—一旦确诊肺结节病,就需要确定其他器官受累的程度。对于经活检确认单器官结节病且没有证据显示其他诊断的患者,有一个工具可用作组织确认结节病累及其他器官的替代指标。结节病可累及的肺外器官系统将单独介绍。除对肺外结节病进行临床和实验室评估外,新诊断为结节病的所有患者均应进行心电图检查。应根据症状、体征和心电图结果来决定是否进行其他检查,例如24小时Holter监测和超声心动图。这些患者还应进行视力检测、眼压测量法、裂隙灯和眼底检查,以评估有无眼部受累。除评估肺外器官受累外,我们还会进行针对维生素D缺乏症的血清检测,通过测量血清25-羟维生素D(骨化二醇)和1,25-二羟维生素D水平实现。几乎所有结节病患者都存在25-羟维生素D缺乏,但是70%的结节病患者1,25-二羟维生素D水平充足。尚不明确结节病患者25-羟维生素D水平低的原因。由于高钙尿症常见,我们可获取随机尿样检测尿钙和肌酐。对于血清钙升高的患者,可收集24小时尿液以评估尿钙排泄和肌酐清除率。如尿液分析显示存在蛋白,则还应在24小时尿样中检测蛋白量。监测—对于结节病,目前并没有关于行特定检查指征和监测疾病活动度最佳频率的资料。初始症状较严重的患者需要更频繁的随访,对于症状轻微或无症状患者,则可降低评估频率。例如,以泼尼松为起始药物治疗活动性疾病的患者需每4-8周重新评估1次,而无症状患者第1年内可每3-4个月随访1次,之后随访间隔延长(通常一年1次)。结节病常规监测项目还包括评估可导致危及器官或生命的肺外组织受累类型,但是尚未正式评估这种监测的有效性。总体指导及检查项目见附表。任何新发症状和用于治疗活动性疾病的在用药物也会影响随访检查项目。并发症—肺结节病偶尔伴有并发症,例如静脉血栓栓塞性疾病(venous thromboembolic disease,VTE)、发生肺曲霉球及肺高压。已有研究报道结节病患者的VTE风险增加。一项人群研究纳入345例新发结节病患者和345例性别、年龄及日历年匹配的对照研究对象,发现在结节病患者中,发生深静脉血栓形成(deep venous thrombosis,DVT)和肺栓塞(pulmonary embolism,PE)的风险增加(分别为:HR 3.04,95%CI 1.47-7.48和HR 4.29,95%CI 1.21-15.23)。对一个大型数据集的分析结果支持上述研究结果,这是IBM Watson Health Explorys的数据集,包含超过2000万例患者,其中超过5.3万例有结节病诊断。校正了性别、年龄和族群后,对于DVT,比值比为3.06(95%CI 2.94-3.18),对于PE,比值比为3.96(95%CI 3.80-4.13)。约2%的结节病患者并发慢性肺曲霉菌病(chronic pulmonary aspergillosis,CPA),该病最常表现为纤维囊性结节病中的肺曲霉球。肺曲霉球也可能并发于空洞性结节病。肺曲霉球的诊断和治疗将单独介绍。在结节病患者中,肺高压一般是晚期肺纤维化的并发症。肺高压与需要辅助供氧有关,但与肺量计检查结果无关。肺部疾病所致肺纤维化的评估和治疗将单独讨论。学会指南链接—部分国家及地区的学会指南和政府指南的链接参见其他专题。患者教育—UpToDate提供两种类型的患者教育资料:“基础篇”和“高级篇”。基础篇通俗易懂,相当于5-6级阅读水平(美国),可以解答关于某种疾病患者可能想了解的4-5个关键问题;基础篇更适合想了解疾病概况且喜欢阅读简短易读资料的患者。高级篇篇幅较长,内容更深入详尽;相当于10-12级阅读水平(美国),适合想深入了解并且能接受一些医学术语的患者。以下是与此专题相关的患者教育资料。我们建议您以打印或电子邮件的方式给予患者。(您也可以通过检索“患者教育”和关键词找到更多相关专题内容。)总结与推荐●结节病是多系统受累疾病,病因未知,病理特征为受累器官存在非干酪样肉芽肿。●结节病的患病率估计为10-20/100,000人。结节病在黑人中比在白人中更常见。黑人更常表现为急性重度疾病,而白人更常表现为轻度慢性疾病。●结节病通常累及年轻成人。约1/2的病例是在无症状人群中因意外发现X线摄影异常(如双侧肺门淋巴结肿大、网状阴影)而检出其患有结节病。结节病常见的主诉症状包括:咳嗽、呼吸困难、胸痛、眼部病变和/或皮损。●应对疑似结节病的所有患者均进行综合评估,包括病史、体格检查、胸片、肺功能测定(PFTs)、外周血细胞计数、血清生化检查、尿液分析、心电图、眼科检查和结核菌素皮肤试验。作此评估的目的是得到更多数据来支持结节病的诊断,以及评估疾病的严重程度和范围,同时排除其他诊断。●肺部影像学检查在结节病诊断中发挥不可或缺的作用,通常首先拍摄胸片,常在随后进行高分辨率计算机断层扫描(HRCT)。其他影像学检查,例如18-FDG-PET和其他放射性示踪剂扫描,是否使用取决于各患者的具体情况。结节病“典型”胸片显示双侧肺门淋巴结肿大。然而,该表现可能不存在,或者与肺实质阴影同时存在。●对疑似结节病的所有患者均应进行PFTs,包括肺量计检查、肺容积、肺弥散量和6分钟步行试验(6MWT),以评价是否有呼吸系统损害,以及是否有特征性的限制性损害伴气体交换减少和功能状态下降。●结节病诊断需要具备以下要素:临床和X线摄影表现符合结节病、排除其他可能表现相似的疾病,以及组织病理学检查发现非干酪样肉芽肿。对于表现为无症状性双侧肺门淋巴结肿大或典型Lofgren综合征[发热、结节性红斑(EN)、关节痛和双侧肺门淋巴结肿大]的患者,如果异常表现迅速自发缓解,则无需活检。●对于大多数疑似结节病患者,应行活检。对容易取样的外周病变(如,皮肤病变、可触及的淋巴结、结膜病变等)行活检优于侵入性操作。如果不能发现易于获取的病变,则操作的选择取决于肺实质异常的模式和位置、胸腔内肿大淋巴结的存在情况和位置,还有现下专业技术和设备。●如果超声引导下内镜或纤维支气管镜检查无法实施或不具诊断性,下一步通常需要进行外科纵隔淋巴结活检,随后是通过胸腔镜或开胸进行外科肺活检。●结节病的典型组织病理学异常为非干酪样肉芽肿。肉芽肿性肺病的鉴别诊断包括很多疾病,尤其重要的是排除感染和恶性肿瘤。本文系张永明医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
张永明 副主任医师 中日医院 呼吸与危重症医学科162人已购买 - 医学科普 慢性阻塞性肺疾病诊治中国指南(2013年修订版)
中华医学会呼吸病学分会慢性阻塞性肺疾病学组中华结核和呼吸杂志2013年4月第36卷第4期慢性阻塞性肺疾病(chronic obstructive pulmonary disease,简称慢阻肺)是一种
张永明 副主任医师 中日医院 呼吸与危重症医学科9881人已读 - 医学科普 中国成人社区获得性肺炎诊断和治疗指南(2016年版)
中华医学会呼吸病学分会中华结核和呼吸杂志2016年4月第39卷第4期本指南的适用范围:年龄18周岁及以上非免疫缺陷的社区获得性肺炎(community-acquiredpneumonia,CAP)患者
张永明 副主任医师 中日医院 呼吸与危重症医学科6万人已读 - 医学科普 咳嗽的诊断与治疗指南(2015)最新版
咳嗽的诊断与治疗指南(2015) 中华医学会呼吸病学分会哮喘学组中华结核和呼吸杂志2016年5月第39卷第5期咳嗽是呼吸专科门诊和社区门诊患者最常见的症状,在国内专科门诊中,慢性咳嗽患者约占三分之一以
张永明 副主任医师 中日医院 呼吸与危重症医学科2万人已读





